Kalsiyum klorür
| Kalsiyum klorür | |
|---|---|
 | |
 | |
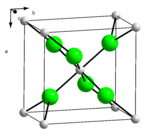
| Kalsiyum klorür | |
| Diğer adlar Kalsiyum(II) klorür, Kalsiyum diklorür, E509 | |
| Tanımlayıcılar | |
| CAS numarası | 10043-52-4 |
| PubChem | 24854 |
| DrugBank | DB01164 |
| ChEBI | 3312 |
| RTECS numarası | EV9800000 |
| ATC kodu | A12,Şablon:ATC, Şablon:ATC |
| SMILES |
|
| InChI |
|
| ChemSpider | 23237 |
| Özellikler | |
| Kimyasal formül | CaCl2 |
| Molar kütle | 110,98 g mol−1 |
| Görünüm | Beyaz toz, higroskopik |
| Koku | Kokusuz |
| Yoğunluk | 2.15 gr/cm3 (susuz) 2.24 gr/cm3 (monohidrat) 1.85 gr/cm3 (dihidrat) 1.83 gr/cm3 (tetrahidrat) 1.71 gr/cm3 (hekzahidrat)[1] |
| Erime noktası |
772-775 °C |
| Kaynama noktası |
1935 °C |
| Çözünürlük (su içinde) | Susuz: 74.5 gr/100 mL (20 °C)[2] Hekzahidrat: 49.4 gr100 mL (−25 °C) 59.5 gr/100 mL (0 °C) 65 gr/100 mL (10 °C) 81.1 gr/100 mL (25 °C)[1] 102.2 gr/100 mL (30.2 °C) α-Tetrahidrat: 90.8 gr/100 mL (20 °C) 114.4 g/100 mL (40 °C) Dihidrat: 134.5 gr/100 mL (60 °C) 152.4 gr/100 mL (100 °C)[3] |
| Çözünürlük () | CH3COOHde çözünür, alkols NH3, DMSO, CH3COOC2H5 sıvısında çözünmez[4] |
| Çözünürlük (etanol içinde) | 18.3 gr/100 g (0 °C) 25.8 gr/100 g (20 °C) 35.3 gr/100 g (40 °C) 56.2 gr/100 g (70 °C)[4] |
| Çözünürlük (metanol içinde) | 21.8 gr/100 g (0 °C) 29.2 gr/100 g (20 °C) 38.5 gr/100 g (40 °C)[4] |
| Çözünürlük (aseton içinde) | 0.1 gr/kg (20 °C)[4] |
| Çözünürlük (piridin içinde) | 16.6 gr/kg[4] |
| Asitlik (pKa) | 8–9 (susuz) 6.5–8.0 (hekzahidrat) |
| Tehlikeler | |
| R-ibareleri | R36 |
| NFPA 704 |
 0
2
|
| LD50 | 1000 mg/kg (sıçan, oral)[5] |
| Belirtilmiş yerler dışında verilmiş olan veriler, standart haldedir. (25 °C, 100 kPa) | |
| Bilgikutusu kaynakları | |
Kalsiyum klorür (CaCl2), kalsiyum ve klorun tuz formudur. Bu bileşik tipik iyonik halojenür gibi hareket eder ve oda sıcaklığında katıdır. Yaygın uygulamaları tuzlu su olarak soğutma tesisleri, yollarda buz ve toz kontrolü ve kurutulması şeklindedir. Higroskopik doğası gereği susuz kalsiyum klorür hava-sızdırmaz kaplar içinde tutulmalıdır.
Ayrıca bakınız
- Kalsiyum(I) klorür
Yararlanılan kaynaklar
- 1 2 Şablon:CRC90
- ↑ "CALCIUM CHLORIDE (ANHYDROUS)". International Programme on Chemical Safety and the European Commission. 25 Eylül 2015 tarihinde kaynağından arşivlendi. http://web.archive.org/web/20150925091632/http://www.inchem.org/documents/icsc/icsc/eics1184.htm.
- ↑ Seidell, Atherton; Linke, William F. (1919). Solubilities of Inorganic and Organic Compounds (2nd bas.). New York: D. Van Nostrand Company. s. 196.
- 1 2 3 4 5 Anatolievich, Kiper Ruslan. "Properties of substance: calcium chloride". 24 Haziran 2015 tarihinde kaynağından arşivlendi. http://web.archive.org/web/20150624025121/http://chemister.ru/Database/properties-en.php?dbid=1&id=558. Erişim tarihi: 2014-07-07.
- ↑
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd bas.). Butterworth-Heinemann. ISBN 0080379419.
| ||||||
This article is issued from Vikipedi - version of the 7/25/2016. The text is available under the Creative Commons Attribution/Share Alike but additional terms may apply for the media files.