Lewis asit ve bazı
Lewis asiti Lewis bazıyla Lewis eklenme ürününü oluşturmak için etkileşen kimyasal türdür. Lewis bazı, Lewis eklenme ürününü oluşturmak için, Lewis asidine elektron çifti veren türdür. Örneğin, OH− ve NH3 Lewis bazlarıdır çünkü bu iyonlar bağ yapmamamış elektron çiftlerini verebilirler. Eklenme ürününde, Lewis asidi ve bazı Lewis bazından gelen elektron çiftini paylaşır.[1] Lewis asit ve bazının isim babası Gilbert N. Lewis'dir.
Eklenme ürünlerinin tasviri
Çoğu durumda, bir kompleksteki Lewis asidi ve bazı arasındaki ilişki, koordine kovalent bağ gösterimi kullanılarak, Lewis bazının Lewis asidine verdiği elektronları gösteren bir ok tarafından belirtilir. Örneğin; Me3B←NH3. Bazı kaynaklar Lewis bazını iki nokta ile birlikte göstererek ifade eder (Bu elektronlar Lewis asitine verilir):
- Me3B + :NH3 → Me3B:NH3
Merkezdeki tek nokta, Lewis eklennme ürününü ifade etmek için kullanılabilir, Me3B•NH3gibi. Başka bir örnek ise BF3•Et2O olabilir. Bahsi geçen nokta aynı zamanda, çeşitli kristallerde hidrat koordinasyonunu belirtmek için kullanılır, MgSO4•7H2O'de hidritlenmiş magnezyum sülfat için olduğu gibi. Genel olarak, donör-alıcı bağı kovalent bağ ve iyonik bağ arasında ideal bir yerde gösterilir.[2]
Örnekler
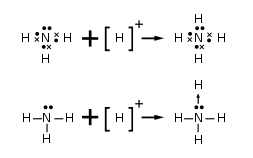
Basit Lewis asitleri
Lewis asitlerinin en çok çalışılan örnekleri boron trihalidler ve organoboranlardır fakat diğer bileşikler aşağıdaki davranışı gösterirler:
- BF3 + F− → BF4−
Bu eklenme ürününde, 4 flor merkezi atomuda eşdeğerdir.
- BF3 + OMe2 → BF3OMe2
BF4− ve BF3OMe2 borontriflorürün eklenme ürünleridir.
Çoğu durumda, triiyodür anyonu gibi, eklenme ürünü oktet kuralını ihlal eder:
- I2 + I− → I3−
İyodür çözeltisinin renk çeşitliliği, çözücünün I2 Lewis asiti ile oluşacak eklenme ürününün çeşitliliğini etkikiler.
Bazı durumlarda,Lewis asitleri 2 Lewis bazını birden bağlama kapasitesine sahiptir. Bunun ünlü bir örneği ise hekzaflorosilikatın oluşumudur:
- SiF4 + 2 F− → SiF62−
Kompleks Lewis asitleri
Çoğu metal kompleks Lewis asidi gibi kullanılırlar fakat genellikle bu durum sadece daha zayıf bir Lewis bazını ayırdıktan sonra geçerlidir, sıklıkla bu baz sudur.
- [Mg(H2O)6]2+ + 6 NH3 → [Mg(NH3)6]2+ + 6 H2O
H+ Lewis asiti
Proton (H+) [3] en güçlü lewis asitlerinden biridir fakat aynı zamanda en karışık olanlardandır.
Lewis bazları
Tipik Lewis bazları amonyak ve alkik aminler gibi alışılagelmiş aminlerdir. Diğer yaygın Lewis bazları ise piridin ve türevlerini içerir.
En yaygın Lewis bazları anyonlardır.
I2, SbCl5, ve BF3 gibi çeşitli Lewis asitleri için hesaplanmış Lewis bazlarının sağlamlığı aşağıda verilmiştir:[4]
| Boron triflorüre bağlanan çeşitli bazların bağlarının sıcaklıkları | ||
|---|---|---|
| Lewis bazı | donör atom | Kompleksleşme Entalpisi (kJ/mol) |
| Et3N | N | 135 |
| quinoklidin | N | 150 |
| piridin | N | 128 |
| Asetonitril | N | 60 |
| Et2O | O | 78.8 |
| THF | O | 90.4 |
| Aseton |
O | 76.0 |
| EtOAc | O | 75.5 |
| DMA | O | 112 |
| DMSO | O | 105 |
| Tetrahidrotiyofen | S | 51.6 |
| Trimetilfosfin | P | 97.3 |
Ayrıca bkz
- Asit
- Baz
- Brønsted–Lowry asit-baz kuramı
- Kiral Lewis asit
Kaynakça
- ↑ http://goldbook.iupac.org/L03508.html
- ↑ March, J. “Advanced Organic Chemistry” 4th Ed. J. Wiley and Sons, 1992: New York.
- ↑ Traditionally, but not precisely, H+ ions are referred as "protons".
- ↑ Christian Laurence and Jean-François Gal "Lewis Basicity and Affinity Scales : Data and Measurement" Wiley, 2009.
Daha fazlası için
- Jensen, W.B. (1980). The Lewis acid-base concepts : an overview. New York: Wiley. ISBN 0-471-03902-0.
- Yamamoto, Hisashi (1999). Lewis acid reagents : a practical approach. New York: Oxford University Press. ISBN 0-19-850099-8.